Seminarium eksperckie nt. umiędzynarodowienia szkół doktorskich

Na świecie miliony ludzi cierpią z powodu niewydolności narządów, a zapotrzebowanie na przeszczepy dramatycznie przewyższa liczbę dostępnych organów od dawców.
W obliczu tej dysproporcji biodruk trójwymiarowy (3D) staje się jedną z najbardziej obiecujących technologii medycyny regeneracyjnej. Perspektywa wytwarzania spersonalizowanych narządów z własnych komórek pacjenta mogłaby nie tylko rozwiązać problem niedoboru dawców, ale również wyeliminować konieczność stosowania toksycznych leków immunosupresyjnych, które są nieodłącznym elementem tradycyjnej transplantologii.
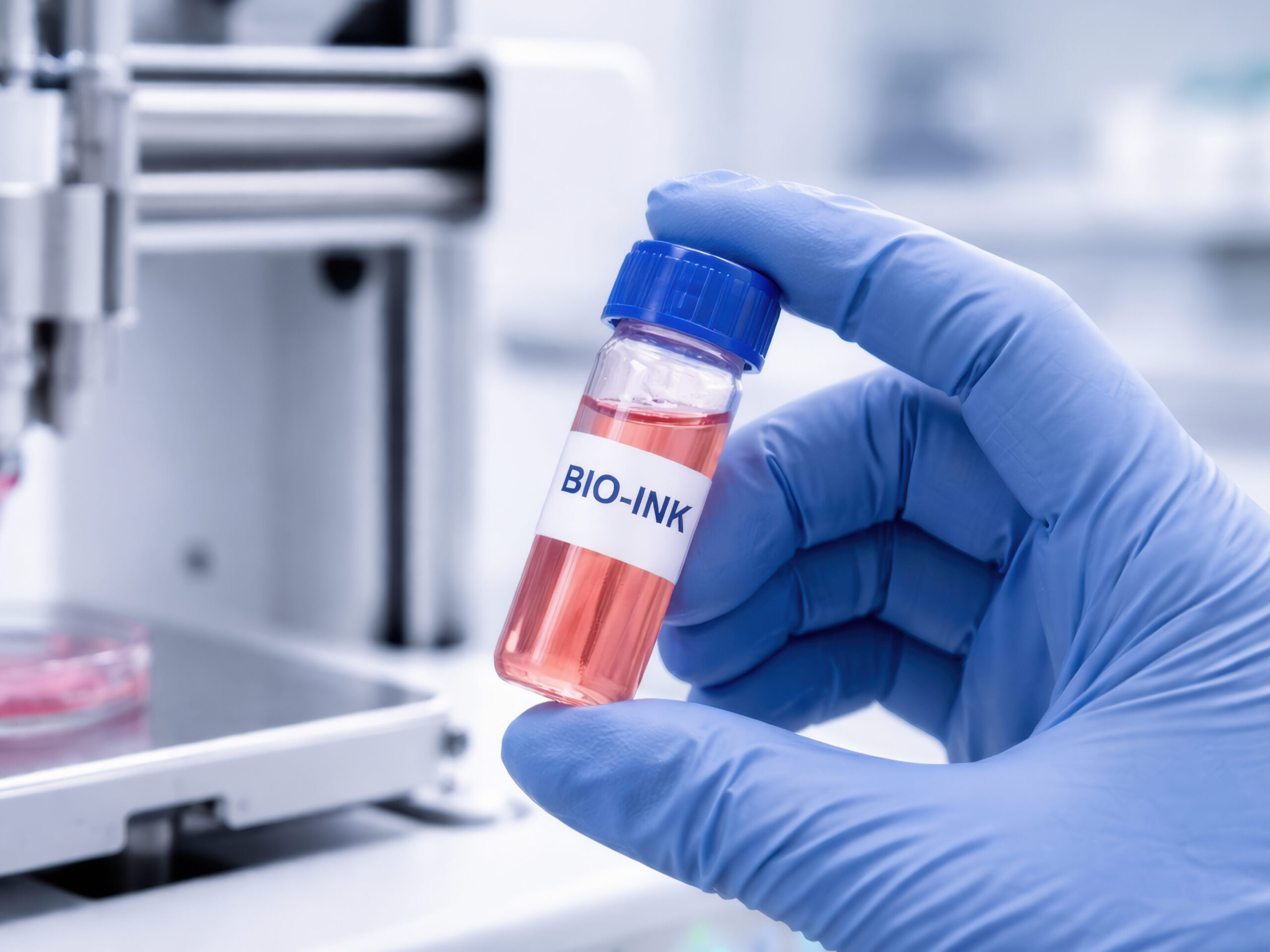
Kluczowym elementem odróżniającym biodruk od klasycznego druku 3D jest zastosowanie w miejsce tworzyw sztucznych tzw. biotuszy (bioinks) – specjalnych preparatów zawierających żywe komórki, białka strukturalne i czynniki wzrostu, które umożliwiają odtworzenie złożonej architektury tkanek biologicznych.
W medycznym biodruku 3D punktem wyjścia jest cyfrowy model narządu przygotowany na podstawie obrazów uzyskanych z tomografii komputerowej lub rezonansu magnetycznego. Na jego bazie oprogramowanie generuje serię bardzo cienkich przekrojów, które drukarka biologiczna kolejno odtwarza, nakładając kolejne warstwy materiału i w ten sposób stopniowo budując trójwymiarową strukturę.
Komórki wykorzystywane w biodruku mogą być pozyskiwane bezpośrednio od pacjenta, co pozwala uzyskać pełną zgodność immunologiczną i eliminuje ryzyko odrzucenia przeszczepu. Źródłem komórek mogą być zarówno komórki zróżnicowane pobierane podczas biopsji, jak i komórki macierzyste – w tym indukowane pluripotentne komórki macierzyste (iPSC), które można wytworzyć z dojrzałych komórek organizmu, a następnie przeprogramować tak, by różnicowały się w praktycznie dowolny typ komórek.
Co istotne, projektowanie modeli narządów oraz analiza danych biologicznych na potrzeby biodruku opierają się dziś w coraz większym stopniu na algorytmach uczenia maszynowego i narzędziach bioinformatycznych – algorytmy AI optymalizują skład biotuszy, monitorują proces druku w czasie rzeczywistym i przewidują zachowanie tkanki po implantacji. To właśnie połączenie biotechnologii i sztucznej inteligencji otwiera zupełnie nowe możliwości medycyny regeneracyjnej.
Bioinformatyka – łącząca biologię molekularną, informatykę i analizę danych – dostarcza przy tym narzędzi do modelowania sekwencji genomowych, doboru odpowiednich komórek macierzystych czy przewidywania zgodności tkankowej. Osoby zainteresowane tą dziedziną mogą rozwijać swoje kompetencje na studiach podyplomowych z Bioinformatyki w PJATK, które łączą wiedzę z zakresu biologii, medycyny i informatyki, lub na nowym kierunku Bioinformatyka – studia II stopnia w PJATK, przygotowującym do pracy badawczo-rozwojowej na przecięciu nauk o życiu i technologii.
We współczesnych biodrukarkach 3D korzysta się już z kilku technik wytwarzania tkanek, z których każda sprawdza się w nieco innych zastosowaniach:
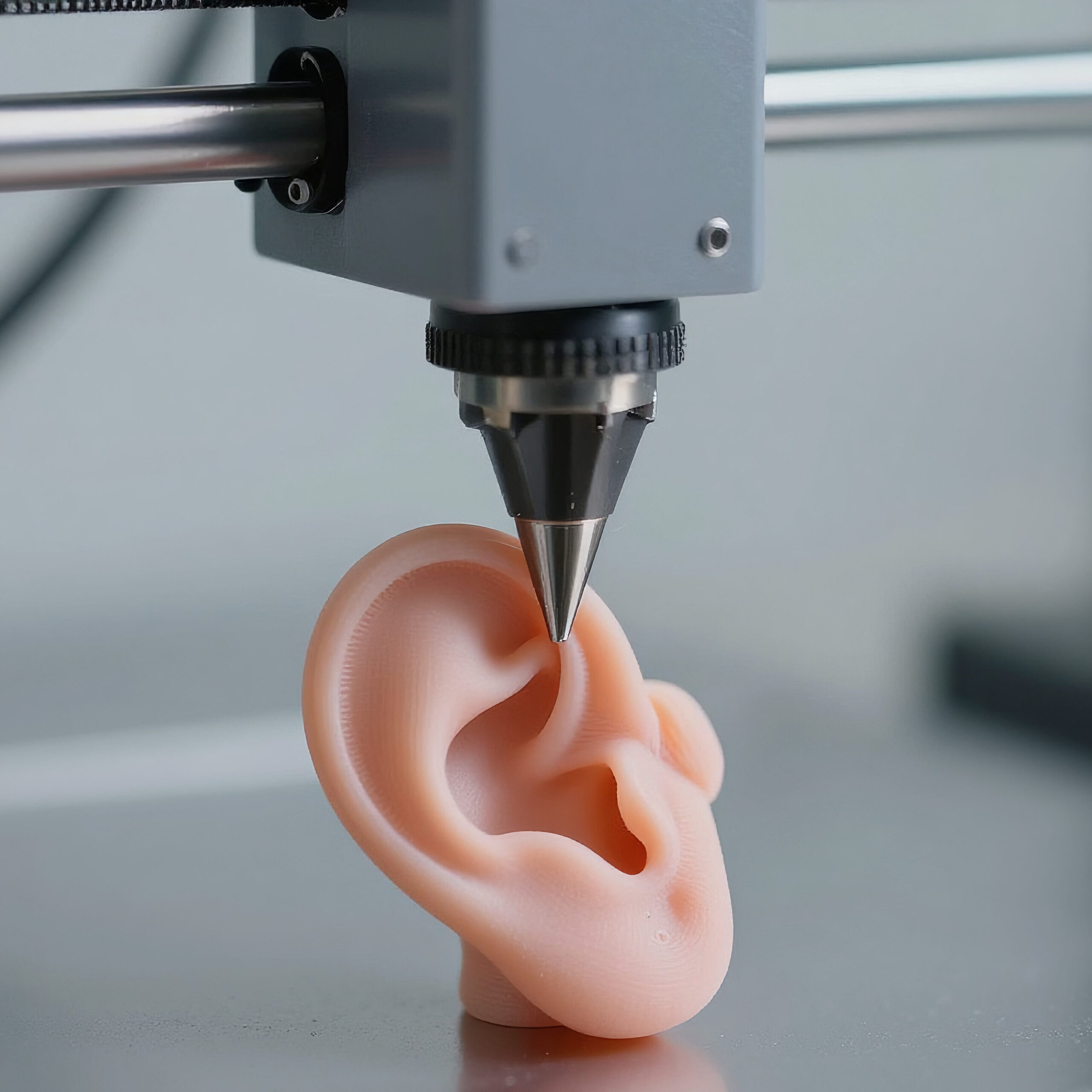
Jednym z najbardziej spektakularnych kamieni milowych biodruku 3D jest implant AuriNovo, opracowany przez firmę 3DBio Therapeutics. W 2022 roku przeprowadzono pierwszy na świecie zabieg wszczepienia biodrukowanego ucha u pacjentki z mikrocją – rzadką wadą wrodzoną polegającą na braku lub niedorozwoju małżowiny usznej.
Implant został wytworzony z własnych chondrocytów (komórek chrząstki) pacjentki, osadzonych w kolagenowym hydrożelu, a jego kształt precyzyjnie odwzorowano na podstawie skanu 3D zdrowego ucha. Amerykańska FDA przyznała AuriNovo status leku sierocego oraz rzadkiej choroby pediatrycznej, a trwające badania kliniczne fazy I/IIa mają na celu potwierdzenie bezpieczeństwa i skuteczności tej metody.
W 2019 roku zespół prof. Tala Dvira z Uniwersytetu w Tel Awiwie wydrukował pierwsze na świecie trójwymiarowe serce zawierające komórki i naczynia krwionośne. Organ – wielkości serca królika – został stworzony z komórek i materiałów biologicznych pobranych od pacjenta.
Naukowcy pozyskali tkankę tłuszczową, z której wyizolowali komórki i przekształcili je w kardiomiocyty oraz komórki śródbłonka, a z macierzy zewnątrzkomórkowej stworzyli hydrożel pełniący rolę biotuszu. Choć wydrukowane serce potrafiło się kurczyć, nie było jeszcze zdolne do skoordynowanego pompowania krwi – kolejnym krokiem stały się więc prace nad opanowaniem synchronicznej pracy komórek i testy na modelach zwierzęcych.
W styczniu 2026 roku agencja ARPA-H (Advanced Research Projects Agency for Health) przyznała zespołowi kierowanemu przez Carnegie Mellon University grant w wysokości 28,5 miliona dolarów na opracowanie biodrukowanej wątroby dla pacjentów z ostrą niewydolnością wątroby.
W ramach tego projektu LIVE (Liver Immunocompetent Volumetric Engineering), wykorzystana zostanie wspomniana już wyżej technika FRESH 3D do drukowania tkanki wątrobowej złożonej wyłącznie z ludzkich komórek i białek strukturalnych, takich jak kolagen. Zaprojektowana wątroba nie ma być trwałym zamiennikiem organu – jej zadaniem jest funkcjonowanie przez 2–4 tygodnie, dając czas na regenerację własnej wątroby pacjenta.
Co jest kluczowe w tym projekcie to fakt, że wątroba jest jedynym narządem wewnętrznym zdolnym do samodzielnej regeneracji, dlatego strategia „mostu czasowego” jest szczególnie obiecująca.
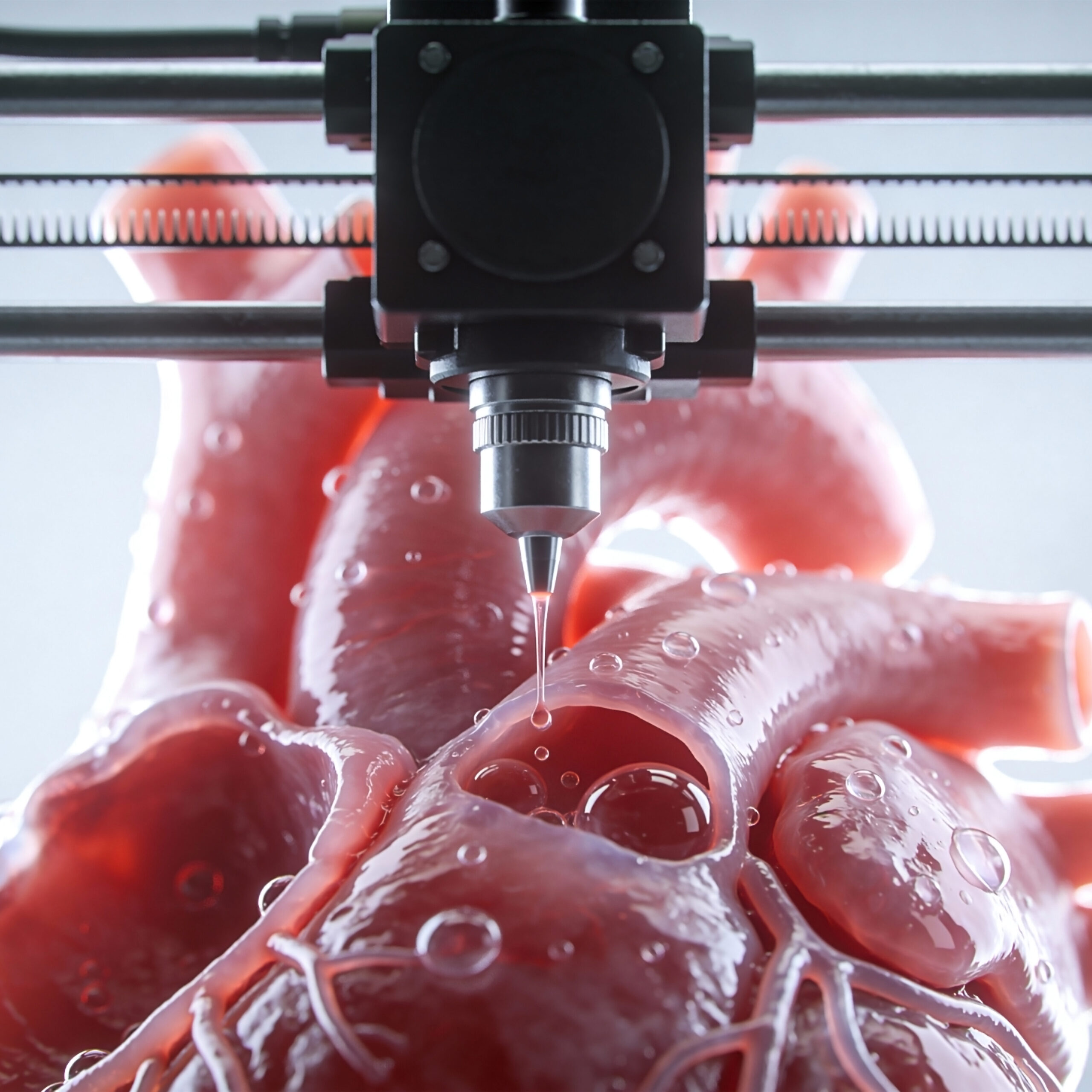
Największą przeszkodą na drodze do biodrukowania pełnowymiarowych narządów pozostaje odtworzenie sieci naczyń krwionośnych. Odwzorowanie hierarchicznej struktury naczyniowej – od dużych tętnic i żył, przez arteriole, po mikroskopijne naczynia włosowate – stanowi fundamentalne wyzwanie inżynieryjne. Bez funkcjonalnej sieci naczyń wydrukowane tkanki szybko obumierają z powodu niedotlenienia.
Wydrukowanie struktury przypominającej narząd to dopiero połowa sukcesu – kluczowe jest osiągnięcie pełnej dojrzałości funkcjonalnej. Komórki muszą nie tylko przeżyć proces drukowania, ale także zorganizować się w prawidłowe struktury tkankowe, nawiązać połączenia nerwowe i zacząć realizować funkcje właściwe danemu narządowi. Na przykład wydrukowane serce musi być zdolne do skoordynowanego bicia, nerka – do filtracji krwi i reabsorpcji, a wątroba – do metabolizowania substancji toksycznych.
Dodatkowo skalowanie technologii z małych modeli laboratoryjnych do pełnowymiarowych narządów ludzkich wiąże się z ogromnymi wyzwaniami logistycznymi – pozyskaniem miliardów komórek czy utrzymaniem ich żywotności podczas wielogodzinnego druku. Sprostanie tym wyzwaniom wymaga specjalistów, którzy łączą kompetencje biologiczne z umiejętnością przetwarzania i analizy wielkich zbiorów danych biologicznych.
Właśnie taką interdyscyplinarną wiedzę oferują studia podyplomowe z Bioinformatyki w PJATK oraz kierunek Bioinformatyka na studiach II stopnia – dla tych, którzy chcą aktywnie uczestniczyć w kształtowaniu przyszłości medycyny regeneracyjnej.
Biodruk 3D w medycynie nie jest już eksperymentalną ciekawostką – to intensywnie finansowana, wielodyscyplinarna dziedzina nauki, która z roku na rok przynosi namacalne postępy. Droga do rutynowego drukowania narządów na życzenie jest jeszcze długa, ale każdy kolejny przełom – od biodrukowanego ucha po program wątroby ARPA-H – przybliża nas do momentu, w którym żaden pacjent nie będzie musiał umierać, czekając na dawcę